Le quitan la “máscara” a mosquito que contagia malaria en Sudamérica
Científicos, entre ellos una académica de la ACFIMAN, secuencian por primera vez el genoma de Anopheles darlingi
Durante millones de años, este mosquito ha estado interpretando a un misterioso personaje que nadie lograba comprender del todo. Finalmente, han podido leer su libreto, el guion donde se revelan cada uno de sus movimientos, motivaciones y artilugios. El susodicho personaje es uno de los principales portadores del parásito que transmite la malaria a los seres humanos y el libreto no es otra cosa que su genoma completo.
Un nuevo estudio, publicado recientemente en la prestigiosa revista Science, describe por primera vez la secuencia total del ADN de Anopheles (Nyssorhynchus) darlingi, el vector de malaria más importante en Sudamérica. La especie anofelina tiene una amplia distribución en el continente americano, que se extiende desde el sur de México hasta el sur de Brasil, “pero su principal hábitat son los bosques tropicales de la región amazónica”, explicó la doctora María Eugenia Grillet, Individuo de Número (Sillón X) de la Academia de Ciencias Físicas, Matemáticas y Naturales de Venezuela (ACFIMAN), profesora e investigadora del Instituto de Zoología y Ecología Tropical de la Facultad de Ciencias de la Universidad Central de Venezuela (IZET-UCV) y coautora del artículo.
Daño colateral
La malaria es una enfermedad que se transmite a los seres humanos por la picadura de mosquitos hembra (principalmente del género Anopheles) infectados con parásitos del género Plasmodium. Según la Organización Mundial de la Salud (OMS), en 2024 la malaria causó 282 millones de casos y 610 000 muertes en 80 países, la gran mayoría en África (95 % de los casos y muertes). En 2023, el 88 % de los casos de malaria en Sudamérica se reportaron en Brasil (30 %), Venezuela (25 %), Colombia (22 %), Guyana (6 %) y Perú (5 %).

La académica de la ACFIMAN recordó que los insectos vectores no transmiten patógenos porque quieran; al contrario, esto es un daño colateral a su característica hematófaga. “Inevitablemente, el parásito ha aprovechado la conducta de los mosquitos de alimentarse de sangre para ‘colarse’ en esa ingesta, ser transmitido a otro hospedador y a la larga sobrevivir”. De hecho, Plasmodium perjudica a An. darlingi, reduciendo su longevidad, supervivencia y capacidad reproductiva; incluso, lo manipula para que pique con mayor frecuencia a los seres humanos y el parásito pueda propagarse mejor.
Tampoco es cierto que todos los mosquitos anofelinos transmiten el parásito de la malaria a los seres humanos. De las 488 especies descritas hasta ahora en el mundo, solo 70 son vectores de Plasmodium y apenas unas 40 se consideran relevantes en la transmisión. “En Sudamérica, se han identificado al menos 11 especies transmisoras de malaria, pero únicamente 4 son vectores importantes, siendo el principal An. darlingi”, precisó la doctora Grillet.
Lamentablemente, y sin proponérselo, An. darlingi “le pone una alfombra roja” a Plasmodium al resistir la invasión y el desarrollo del parásito dentro de él. También es una especie que se adapta rápidamente a los cambios ambientales ⏤“por eso es común en áreas de bosque perturbadas por la minería”, comentó la investigadora⏤, y puede alimentarse de sangre humana dentro o fuera de las viviendas.
“Debilidad” por la sangre humana
Para el estudio publicado el pasado mes de marzo en Science, dirigido por la Escuela de Salud Pública TH Chan de Harvard (Boston, Massachusetts, Estados Unidos), los investigadores generaron secuencias del genoma de 1094 hembras adultas de An. darlingi procedentes de 16 localidades (bosques, pastizales, zonas agrícolas y mineras, humedales y áreas rurales) en 6 países sudamericanos (Guayana Francesa, Brasil, Guyana, Perú, Venezuela y Colombia). Nunca se habían secuenciado tantos genomas completos de Anopheles.
Aunque los mosquitos anofelinos se alimentan de la sangre de otros animales ⏤lagartos, serpientes, aves, mamíferos y primates no humanos⏤, algunos tienen preferencia por la sangre humana, especies que, a fin de cuentas, terminan convirtiéndose en vectores de patógenos que infectan a los propios humanos. La doctora Grillet informó que en este trabajo analizaron el contenido estomacal de An. darlingi para determinar cuánta sangre humana y de otros vertebrados habían ingerido. Los resultados muestran que casi la mitad de los restos sanguíneos hallados en los mosquitos eran humanos, por delante de perros, búfalos, bueyes, gallos y murciélagos.
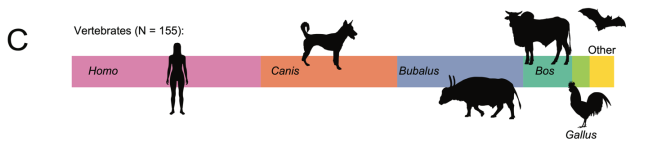
Fuente: Tennessen, J. A. et al., 2026
Unidos por el agua
Otro hallazgo revelador fue la heterogeneidad genética de las poblaciones de mosquitos, consecuencia de las profundas divisiones geográficas. “Lo más sorprendente e interesante es que esa heterogeneidad viene dada principalmente por los límites de las cuencas hidrográficas, más que por barreras físicas obvias que impiden el flujo genético”, aseguró la académica de la ACFIMAN. Es decir, el ADN de los mosquitos resultó igual al de otros que viven a varias decenas de kilómetros, pero que comparten la misma cuenca.

Por lo general, los animales se mantienen aislados genéticamente cuando hay una montaña o río gigante que no pueden cruzar. Para An. darlingi, el río, en lugar de representar un obstáculo, viene a ser como una “autopista”. A los mosquitos del municipio Sifontes (Bolívar, Venezuela) les queda más cerca Guyana o Guayana Francesa en el mapa. Sin embargo, su ADN dice que son parientes de los mosquitos de Amazonas (Venezuela) y Guainía (Colombia), ambos pertenecientes a la región de la Orinoquia. Esto tiene todo el sentido del mundo, ya que, antes de volar y picar a las personas, los mosquitos pasan sus primeras etapas de vida (huevo y larva) en el agua. Al criarse en las orillas de los ríos, su destino está ligado a la corriente.
Además de las vías fluviales, la conectividad entre poblaciones de mosquitos “puede verse mejorada por la actividad antropogénica a lo largo de los ríos, incluyendo la deforestación que conduce a un hábitat perturbado favorable o el transporte en vehículos o barcos” (Tennessen, J. A. et al., 2026).
Pros y contras de la diversidad
A diferencia de los vectores africanos, An. darlingi en Sudamérica es una sola especie morfológica sin evidencia de taxones crípticos (especies idénticas pero genéticamente aisladas), lo que simplifica la identificación taxonómica para los programas de control. A pesar de ello, se encontró que en An. darlingi la diversidad genética es excepcionalmente alta, superando incluso a sus parientes lejanos, los vectores africanos. Esta “biblioteca genética” le otorga al mosquito una gran capacidad de adaptación ante transformaciones ambientales o nuevas intervenciones sanitarias.
La divergencia genética tiene puntos positivos y negativos.
Por el lado negativo, destaca el control efectivo de la malaria. Como no todos los mosquitos portadores del parásito transmisor de la infección son iguales por dentro (genéticamente hablando), las estrategias de salud tienen que ser locales, ya que lo que pudiera eliminar al mosquito en un lugar podría no funcionar en otro. Del lado positivo, figura la resistencia “contenida” a los insecticidas. “Es menos probable que el alelo de resistencia a los insecticidas se propague rápidamente más allá de su población de origen”, afirman los autores en la publicación.
En otras palabras, no habría probabilidad de que la mutación que genera resistencia a los insecticidas en la Guayana Francesa se disperse al municipio Sifontes (Bolívar, Venezuela), a pesar de compartir frontera, “lo que es una buena noticia”, aclaró la doctora Grillet.
Resistencia a insecticidas

La mala noticia es que An. darlingi está mostrando señales de resistencia emergente a los insecticidas. “Hay evolución en marcha, porque observamos fijación de mutaciones resistentes a los insecticidas”, explicó la científica.
Esta especie anofelina ha sido capaz de adaptarse a cambios ecológicos y demográficos antropogénicos, como el uso de insecticidas para el control de plagas en cultivos, el empleo de mosquiteros impregnados con insecticidas de larga duración y la deforestación con fines agrícolas, urbanísticos o mineros. No obstante, las indicaciones de resistencia a los insecticidas no se detectaron en todas las áreas analizadas, sino en regiones particulares (Colombia y Guayana Francesa) donde estas presiones ambientales han sido mayores, precisó.
¿De qué manera el monitoreo genómico continuo de las poblaciones de mosquitos puede contribuir a los esfuerzos de control de enfermedades? De acuerdo con la doctora Grillet, “estudiar el genoma de los mosquitos vectores de Plasmodium permitiría identificar genes que regulan la capacidad de transmitir la malaria, desarrollar métodos de control más efectivos y diseñar intervenciones innovadoras y sofisticadas, como el uso de mosquitos genéticamente modificados (transgénicos) y resistentes al parásito”.
Por Venezuela, además de la doctora Grillet, figura como coautor del artículo el doctor Jorge E. Moreno, entomólogo del Centro de Investigación Francesco Vitanza (Tumeremo, Bolívar) del Instituto Altos Estudios Dr. Arnoldo Gabaldón, adscrito al Ministerio del Poder Popular para la Salud.
MMS Américas
En vista de que la resistencia a los insecticidas puede evolucionar de forma paralela en diferentes regiones bajo presiones ambientales similares, la académica de la ACFIMAN cree imperativo establecer una red de monitoreo genómico continuo para anticiparse a los brotes de malaria. “Derrotar a la malaria requiere una colaboración internacional sin precedentes que combine la ciencia de vanguardia con el trabajo de campo”, dijo.
Desde 2025, funciona MMS Américas, una red de científicos, instituciones y agencias de salud pública que trabajan coordinadamente para fortalecer la vigilancia molecular de la malaria (malaria molecular surveillance, MMS) en América Latina y el Caribe, a través del intercambio de datos, la estandarización de protocolos y el desarrollo de capacidades. “Nuestro estudio en Science es un comienzo”, auguró investigadora ucevista.
Teniendo el guion en su poder, la ciencia puede alterar la historia de ese temido personaje.
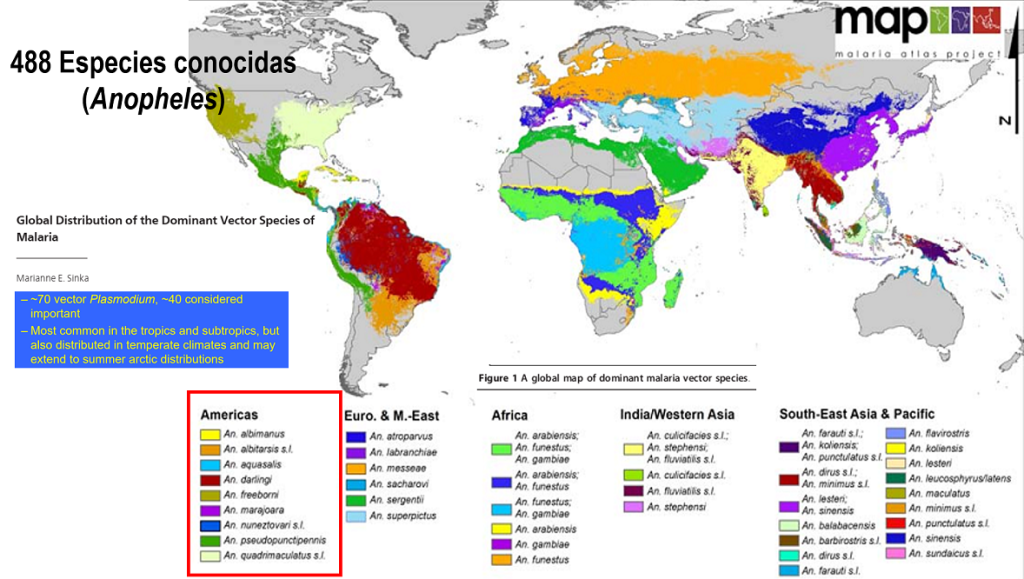
Fuente: Sinka, M. E. (2013). Global Distribution of the Dominant Vector Species of Malaria. En S. Manguin (Ed.), Anopheles mosquitoes – New insights into malaria vectors (pp. 109-144). IntechOpen. https://doi.org/10.5772/55267
Referencia:
Tennessen, J. A. et al. (2026). Population genomics of Anopheles darlingi, the principal South American malaria vector mosquito. Science 391, 1373-1378. DOI: 10.1126/science.adw9761